Catéchine
| Catéchine | |

| |
| (+)-Catéchine | |
| Identification | |
|---|---|
| Nom UICPA | ()-2-(3,4-dihydroxyphenyl)chromane-3,5,7-triol |
| Synonymes |
catéchol, cianidanol |
| No CAS | |
| No ECHA | 100.005.297 |
| No CE | 205-825-1 |
| SMILES | |
| Propriétés chimiques | |
| Formule | C15H14O6 [Isomères] |
| Masse molaire[1] | 290,268 1 ± 0,014 8 g/mol C 62,07 %, H 4,86 %, O 33,07 %, 290,27 |
| Propriétés physiques | |
| T° fusion | 214 °C |
| Solubilité | 6,31 mg·l-1 |
| Écotoxicologie | |
| DL50 | 10 mg·kg-1, rat, oral |
| Composés apparentés | |
| Autres composés | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La catéchine est un composé organique de la famille des flavanols, une sous-classe des flavonoïdes. Elle est aussi connue sous le nom de catéchol, avec le risque de confusion avec le pyrocatéchol parfois dénommé lui aussi catéchol. L'usage dans la communauté scientifique a fini par imposer le terme de catéchine, dérivé du terme anglais catechin. Ce tannin catéchique est un composé allélopathique initialement découvert dans les fruits de l'acacia à cachou (Acacia catechu, auquel cette molécule doit son nom). La catéchine et ses nombreux isomères sont de puissants antioxydants qui aident à prévenir les maladies inflammatoires et coronariennes. Ils sont également phytotoxiques et antibactériens[2].
Le terme de catéchine est aussi parfois utilisé pour désigner la classe des flavanols (flavan-3-ols, flavan-3,4-ols et leurs esters galliques). Pour éviter la confusion entre la classe et le composé, ce dernier est désigné dans ce contexte par (+/-)-catéchine.
Les stéréoisomères
[modifier | modifier le code]
La catéchine existe sous forme de plusieurs stéréoisomères provenant de deux carbones asymétriques. Les formes énantiomères (en image spéculaire) dans les positions 2 et 3 de l'hétérocycle central, nommée configuration R/S, donnent les quatre structures suivantes[3] :
| Structures des énantiomères de la catéchine/épicatéchine | ||
| Nom | Configuration | Formule |
|---|---|---|
| (+)-catéchine | 2R, 3S | 
|
| (–)-épicatéchine | 2R, 3R | 
|
| (–)-catéchine | 2S, 3R | 
|
| (+)-épicatéchine | 2S, 3S | 
|
Dans la nature, les isomères les plus fréquents sont la (+)-catéchine et la (–)-épicatéchine. Les deux autres énantiomères sont beaucoup plus rares et leur présence semble liée à des réactions enzymatiques ou à des traitements thermiques.
C'est ainsi que la fève de cacao fraîche contient principalement de la (–)-épicatéchine et un peu de (+)-catéchine. Mais une fois torréfiée, la fève (et le chocolat) révèle en plus de la (–)-catéchine. La haute température nécessaire à la torréfaction déplace l'équilibre d'épimérisation vers la (–)-catéchine :
(–)-épicatéchine → (–)-catéchine
Certaines plantes synthétisent en égales quantités les énantioméres (+) et (–). Ainsi, la racine de centaurée maculée[4] (Centaurea maculata) exsude une (±)-catéchine racémique avec une composante (–)-catéchine développant une activité herbicide puissante, susceptible de repousser les plantes voisines compétitives.
Le chauffage de la catéchine au-delà de son point de décomposition libère du pyrocatéchol, dénommé aussi catéchol, au risque de confusion.
Les tanins condensés sont des oligomères ou des polymères dérivés de la (+)-catéchine ou de ses isomères.
Quelques catéchines communes
[modifier | modifier le code]Catéchines communes du thé et du vin avec une configuration –cis dans les positions 2, 3 :
| Structures de catéchines 2,3-cis | |||
| Composés | R3 | R5' | Structures |
|---|---|---|---|
| (–)-épicatéchine EC | OH | H | 
|
| (–)-épigallocatéchine EGC | OH | OH | |
| (–)-épicatéchine gallate ECG | G | H | |
| (–)-épigallocatéchine gallate EGCG | G | OH | |
Quelques catéchines communes avec une configuration -trans dans les positions 2, 3 :
| Structures de catéchines 2,3-trans | |||
| Composés | R3 | R5' | Structures |
|---|---|---|---|
| (+)-catéchine C | OH | H | 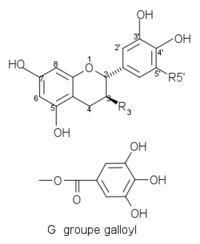
|
| (+)-gallocatéchine GC | OH | OH | |
| (+)-gallocatéchine gallate GCG | G | OH | |
Inhibition de l'histidine décarboxylase
[modifier | modifier le code]La (+)-catéchine est un inhibiteur de l'histamine N-méthyl transférase, et inhibe donc la conversion de la L-histidine en histamine. De ce fait, elle peut avoir un effet bénéfique sur les désordres immuns dus à l'histamine dans un certain nombre de pathologies dont, entre autres, l'ulcère gastrique[5].
Action générale sur la santé
[modifier | modifier le code]L'action générale des catéchines sur la santé est mal connue, elles font partie des anti-oxydants, mais on considère parfois qu'elles pourraient limiter l'absorption du fer[6],[7].
Catéchines et métaux lourds
[modifier | modifier le code]Des catéchines (celles du thé notamment) semblent diminuer le stress oxydatif induit par le plomb dans les cellules[8]. Elles pourraient donc participer au traitement des intoxications saturnines.
Notes et références
[modifier | modifier le code]- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ (en) Bais HP, Walker TS, Stermitz FR, Hufbauer RA, Vivanco JM, « Enantiomeric-dependent phytotoxic and antimicrobial activity of (±) catechin. A rhizosecreted racemic mixture from spotted knapweed », Plant Physiology, vol. 128, no 4, , p. 1173-1179 (DOI 10.1104/pp.011019)
- ↑ (en) Michael Kofink, Menelaos Papagiannopoulos and Rudolf Galensa, « (–)-Catechin in Cocoa and Chocolate: Occurrence and Analysis of an Atypical Flavan-3-ol Enantiomer », Molecules, vol. 12, , p. 1274-1288
- ↑ (en) Harsh Pal Bais, Travis S. Walker, Frank R. Stermitz, Ruth A. Hufbauer, and Jorge M. Vivanco, « Enantiomeric-Dependent Phytotoxic and Antimicrobial Activity of (–)-Catechin. A Rhizosecreted Racemic Mixture from Spotted Knapweed », Plant Physiology, vol. 128, , p. 1173-1179
- ↑ Histamine and acute haemorrhagic lesions in rat gastric mucosa: Prevention of stress ulcer formation by (+)-catechin, an inhibitor of specific histidine decarboxylase in vitro. H. -J. Reimann, W. Lorenz, M. Fischer, R. Frölich, H. -J. Meyer and A. Schmal, Inflammation Research, Volume 7, Number 1 / march 1977, Pages 69-73, DOI 10.1007/BF01964883
- ↑ LES CATÉCHINES ET LA SANTÉ : Etat des Connaissances
- ↑ Green tea or rosemary extract added to foods reduces nonheme-iron absorption
- ↑ Chen, L., Yang, X., Jiao, H., & Zhao, B. (2002). http://toxsci.oxfordjournals.org/content/69/1/149.full Tea catechins protect against lead-induced cytotoxicity, lipid peroxidation, and membrane fluidity in HepG2 cells]. Toxicological sciences, 69(1), 149-156.
Article connexe
[modifier | modifier le code]- Flavan-3-ol
- Lutéoliflavane ou 3-déoxycatéchine
Liens externes
[modifier | modifier le code]
- Ressources relatives à la santé :
- Notice dans un dictionnaire ou une encyclopédie généraliste :
Estimation de l'apport en catéchines et procyanidines relatif à une consommation modérée et régulière de vins en France, Carando S., Teissedre P. L., et Cabanis J. C. du Centre de formation et de recherche en œnologie, Faculté de pharmacie, Montpellier.
