Inhibiteur de l'enzyme de conversion
| Inhibiteur de l'enzyme de conversion | |
| |
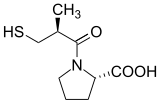
| Le captopril, première molécule de cette classe commercialisée pour le traitement de l'hypertension artérielle | |
| Identification | |
|---|---|
| Code ATC | ATC C09AA |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Les inhibiteurs de l’enzyme de conversion (IEC) sont des médicaments, qui sont utilisés notamment dans le traitement de l’hypertension artérielle, de la maladie coronarienne et de l’insuffisance cardiaque chronique. Ce sont des inhibiteurs de l’enzyme de conversion de l’angiotensine (ECA souvent abrégée ACE du fait de l'acronyme anglophone angiotensin-converting enzyme), qui est un élément d’une cascade régulant la pression artérielle (système Rénine-Angiotensine-Aldostérone). Les composants inhibant l’ECA ont été trouvés initialement dans le venin de serpents du genre Bothrops.
Les principaux représentants utilisés dans le domaine thérapeutique sont le captopril, l’énalapril, le lisinopril et le ramipril. Compte tenu de leur forte importance thérapeutique, ces médicaments font partie des substances ayant généré les chiffres d’affaires les plus élevés.
Chimie
[modifier | modifier le code]
Les inhibiteurs de l’ECA tels que le captopril, l’énalapril et leurs substances successeurs ont une structure apparentée à celle du peptide isolé à partir du venin du serpent brésilien Jararaca - fer de lance (Bothrops jararaca), BPP5a (Peptide"" potentialisant la Bradykinine; voir figure). La séquence de tripeptides présente dans BPP5a et se composant de trois acides aminés Tryptophane-Alanine-Proline a été identifiée comme le composant efficace (représenté en rouge sur la figure).
Étant donné que BPP5a et le tripeptide sont dégradés très rapidement dans le corps, de nombreuses modifications ont été effectuées sur la molécule, afin de prolonger la durée d’action. À cette fin, la séquence tryptophane-alanine-proline a été échangée contre une séquence similaire mais plus stable phénylalanine-alanine-proline. L’intégration d’une structure analogue acide Bernstein ou acide glutarique (représenté en vert sur la figure) a apporté une stabilité plus importante et un renforcement de l’inhibition à l’enzyme de conversion de l’angiotensine.
Par ailleurs, à l’exception du captopril et du lisinopril, tous les inhibiteurs de l’ECA utilisés en thérapeutique sont des prodrogues, qui ne sont activés que dans l’organisme. Dans le cas de l’énalapril, ceci se produit par la scission du groupe éthyl par les estérases, la forme active, l’énalaprilate étant formée avec un groupe carboxyle libre.
Pharmacologie
[modifier | modifier le code]Indications
[modifier | modifier le code]Les inhibiteurs de l’ECA sont utilisés principalement dans le traitement de l’hypertension artérielle. Ils sont considérés, soit seuls (en monothérapie), soit en association avec d’autres anti-hypertenseurs (Traitement combiné, notamment avec un diurétique ou un antagoniste calcique) comme un traitement de première intention. Dans les formes d’hypertension qui s’accompagnent d’un faible taux de rénine dans le plasma sanguin (par exemple Syndrome de Conn), les inhibiteurs de l’ECA ne montrent, en revanche, qu’une efficacité limitée[1].
Dans l'insuffisance cardiaque de type systolique, les inhibiteurs de l’ECA améliorent les symptômes, allongent la vie et en diminuent les complications. Cette propriété repose vraisemblablement sur la baisse de la post-charge et la diminution de la tension de la paroi du muscle cardiaque du fait de la baisse de l’angiotensine II[2].
Les mêmes propriétés sont retrouvées pour le traitement de la maladie coronarienne, par exemple après un infarctus du myocarde. Cependant, en cas de coronaropathie en l'absence d'insuffisance cardiaque, leur intérêt semble négligeable[3].
La néphropathie diabétique est une autre indication des inhibiteurs de l’ECA.
En médecine vétérinaire, les inhibiteurs de l'ECA sont également utilisés lors d'insuffisance cardiaque canine ou d'insuffisance rénale chez le chat.
- Les IECA sont indiqués dans l’insuffisance rénale chronique du chat dans la mesure où le rapport protéine urinaire/créatinine urinaire est supérieur à 0,4. Les paramètres sanguins (urémie et créatininémie) sont susceptibles d'augmenter dans une première phase (10-12jours). Cet effet semble être lié à la diminution de l'hypertension rénale rapidement compensée par une amélioration du rendement des néphrons. Le contrôle de ces paramètres sanguins est donc conseillé pour connaitre l'impact du traitement, la nécessité de le poursuivre ou de combattre ses effets néfastes momentanés.
Mécanisme d’action
[modifier | modifier le code]Le mécanisme d’action moléculaire des inhibiteurs de l’ECA repose sur la similitude des inhibiteurs de l’ECA avec une fin de chaîne peptidique de l’angiotensine I. De ce fait, les inhibiteurs de l’ECA sont considérés par erreur par l’Enzyme de conversion de l’angiotensine comme le substrat physiologique angiotensine I. À la différence du substrat physiologique, ils ne sont cependant pas transformés par l’enzyme et bloquent cette dernière.
Le mécanisme d’action des inhibiteurs de l’ECA repose sur une inhibition de l’enzyme de conversion de l’angiotensine. Cette enzyme assume deux missions principales dans l’organisme. D’une part, elle est compétente pour la synthèse de l’octapeptide actif sur la vasoconstriction (peptide composé de 8 acides aminés) l’angiotensine II, à partir de son précurseur inactif, le décapeptide (10 acides aminés) l’angiotensine I en scindant les deux acides aminés C terminaux. D’autre part, elle favorise la dégradation de la bradykinine. L'utilisation d'inhibiteurs de l'ECA provoque donc une accumulation de bradykinine, qui sera responsable d'une partie de ses effets indésirables.
L’inhibition de l’enzyme de conversion de l’angiotensine entraîne une diminution de la concentration d’angiotensine II au niveau des récepteurs de l’angiotensine (AT1 et AT2). Premièrement, de ce fait, le tonus vasculaire diminue et la pression artérielle baisse. Deuxièmement, la baisse des taux d’angiotensine II induit une diminution de la libération d’aldostérone de la corticosurrénale et donc un effet sur le bilan hydrique (voir aussi Système Rénine-Angiotensine-Aldostérone). Au niveau cellulaire, on peut observer une baisse des effets mitogènes médiés par l’angiotensine II sur les fibroblastes et les myocytes du cœur, qui conduisent, notamment après un infarctus, à des changements défavorables (remodelage).
En cas de pathologies rénales telles que la néphropathie diabétique, les inhibiteurs de l’ECA entraînent une excrétion réduite des protéines (protéinurie) et empêchent toute progression de l’affection (néphroprotection).
L’inhibition de la dégradation de la bradykinine entraîne en revanche son accumulation et ses effets indésirables associés.
Pharmacocinétique
[modifier | modifier le code]Conformément à leurs différences chimiques, les inhibiteurs de l’ECA se distinguent par leur pharmacocinétique. La majorité des inhibiteurs de l’ECA actuellement disponibles sont des prodrogues. Cela signifie qu’ils doivent être activés, après une absorption (résorption) de 20 % (ramipril) à presque 100 %, par les enzymes dans le corps (voir Chimie). Seuls le captopril et le lisinopril n’ont pas besoin de cette phase d’activation. Les concentrations plasmatiques maximales des formes actives sont atteintes après 1 à 8 heures. Les demi-vies plasmatiques varient entre 2 (captopril) et 40 heures (spirapril (en)). Leur durée d’action varie en conséquence (de 8 à 48 heures). Tous les inhibiteurs de l’ECA sont essentiellement éliminés par les reins. Le fosinopril, moexipril et spirapril présentent par ailleurs une excrétion biliaire pertinente (élimination par la bile).
Actions
[modifier | modifier le code]Outre la baisse du niveau tensionnel, ils permettent de diminuer la morbidité ou la mortalité cardio-vasculaire, que cela soit chez le patient avec insuffisance cardiaque ou sans. Dans ce dernier cas, cela a été démontré essentiellement chez les patients à hauts risque vasculaires avec le ramipril[4], le périndopril[5] et l'énalapril[6]. D'autres inhibiteurs de l'ECA ont été testées, retrouvant pour la plupart, une tendance à une réduction de la morbidité, sans que cela atteigne le seuil de significativité. Globalement, les inhibiteurs de l'ECA semblent diminuer cette morbidité, avec une baisse de la mortalité[7].
Effets indésirables
[modifier | modifier le code]Les principaux effets indésirables des inhibiteurs de l’ECA sont associés à une dégradation et accumulation plus lentes de la bradykinine par les inhibiteurs de l’ECA. En font partie les réactions cutanées, par exemple l’exanthème (0,1 - 1 %) et l’urticaire (0,01 - 0,1 %). Les réactions allergiques sévères ne sont en revanche observées que très rarement (< 0,01 %). L’effet indésirable considéré comme caractéristique des inhibiteurs de l’ECA (ainsi que des Sartans et des inhibiteurs de la rénine), à savoir la survenue d’un angio-œdème héréditaire[8], peut de même être observé dans de rares cas (0,01 - 0,1 %) et dont les symptômes peuvent être pris en charge par l'administration d'Icatibant, de Danazol, d'inhibiteur de la C1 ésterase ou son analogue recombinant le Conestat alfa.
La majorité des effets indésirables concernant les voies respiratoires peut aussi être associée à l’accumulation de bradykinine. Ces effets fréquents (1% à 10%) et ont une gravité modérées à sévères[9]. On peut citer la toux sèche (supérieur à 10%)[8], l’enrouement et les maux de gorge (0,1 - 1 %). Des crises d’asthme et une détresse respiratoire peuvent survenir, même si cela est rare (0,01 - 0,1 %).
Sous traitement par les inhibiteurs de l’ECA on peut observer, indépendamment de la bradykinine, une baisse trop forte de la pression artérielle. En conséquence, des vertiges, céphalées et étourdissements peuvent occasionnellement survenir (0,1 - 1 %)[8]. Des cas isolés d’événements cardiovasculaires, tels que angine de poitrine, infarctus et syncope, ont été rapportés.
Du fait de l’intervention dans le bilan hydrique et électrolytique, une insuffisance rénale peut occasionnellement être observée (0,1 - 1 %). Une protéinurie (excrétion de protéines dans les urines) n’a cependant été rapportée que dans de rares cas (0,01 - 0,1 %). Les actions sur le système rénine-angiotensine-Aldostérone, avec diminution de la distribution d’aldostérone permettent d’expliquer un autre effet indésirable des inhibiteurs de l’ECA : L’aldostérone renforce la recapture de Na+ et d’eau dans les reins, tandis qu’elle favorise l’élimination du potassium. En cas de concentration réduite d’aldostérone, on peut assister à l’effet contraire : élimination plus élevée du sodium et de l’eau par le rein, tandis que le potassium s’accumule dans l’organisme. Ainsi, il peut en résulter une hyperkaliémie dangereuse, essentiellement pour le cœur[8]. De rares cas d’hyponatrémie ont été observés.
Les inhibiteurs de l’ECA peuvent, pendant le premier trimestre de la grossesse, augmenter le risque de malformations cardiaques et neurologiques[10], mais, en fait, pas plus que les autres traitements antihypertenseurs ce qui peut faire poser la question du risque propre de l'hypertension artérielle chez la femme enceinte[11]. Ils restent contre-indiqués pendant la grossesse et doivent être remplacés par d’autres mesures thérapeutiques appropriées[12].
Leur utilisation est associé avec une faible augmentation du risque de survenue d'un cancer du poumon[13].
Interactions médicamenteuses
[modifier | modifier le code]Les inhibiteurs de l’ECA renforcent les effets indésirables des médicaments immunosuppresseurs (immunosuppresseurs, cytostatiques et glucocorticoïdes) au niveau de l’hémogramme. De même, les inhibiteurs de l’ECA majorent l’action hypoglycémiante d’un antidiabétique oral et de l’insuline.
La modification du bilan hydrique et électrolytique peut ralentir l’élimination du lithium. De même, on peut observer une augmentation plus importante des concentrations de potassium en cas d’utilisation concomitante de diurétiques épargnant le potassium.
En cas d’association avec d’autres médicaments hypotenseurs, il faut tenir compte d’une hypotension renforcée. Les effets synergiques, qui peuvent être utilisés sur le plan thérapeutique, apparaissent notamment avec les diurétiques et les inhibiteurs des canaux calciques. Un effet hypotenseur réduit des inhibiteurs de l’ECA a pu être observé dans des cas isolés après la prise d’aliments riches en sel.
Il existe une augmentation du risque de survenue d'une insuffisance rénale aiguë en cas d’association avec un diurétique et un anti-inflammatoire non stéroïdien[14].
Médicaments
[modifier | modifier le code]Actuellement, les inhibiteurs de l’ECA suivants sont autorisés comme médicaments :
- bénazépril (Cibacen, Lotensin, génériques) ;
- captopril (Lopril, Tensobon, Capoten, nombreux génériques) ;
- cilazapril (Dynorm, Inhibace) ;
- énalapril (Xanef, Pres, Renitec, Vasotec, nombreux génériques) ;
- fosinopril (Fosinorm, Dynacil, Monopril, génériques) ;
- lisinopril (Zestril, Acerbon, Coric, génériques) ;
- midapril (Tanatril) ;
- moexipril (Fempress) ;
- périndopril (Coveram, Coversyl, Preterax, génériques) ;
- quinapril (Accupro, Accupril, génériques) ;
- ramipril (Triatec, Delix, Vesdil, Altace, génériques) ;
- spirapril (en) (Quadropril) ;
- trandolapril (Gopten, Mavik, Odrik, Udrik, génériques) ;
- zofénopril (Zofénil, génériques).
Historique
[modifier | modifier le code]La première pierre du développement des inhibiteurs de l’enzyme de conversion de l’angiotensine (ECA) a été posée en 1956 avec l’explication de la fonction de l’enzyme de conversion de l’angiotensine (ECA) par Leonard T. Skeggs. Le rôle de cette enzyme dans la régulation de la pression artérielle a été largement sous-estimée dans les premiers temps.
En 1970, soit 14 ans après la découverte de l’enzyme de conversion de l’angiotensine (ECA), le pharmacologue Sergio H. Ferreira a lui-même observé que le venin du serpent Jararaca fer de lance entraînait in vitro une inhibition de cette enzyme. Un des composants efficaces a été alors isolé avec le pentapeptide BPP5a contenu dans ce venin de serpent.
Étant donné que le pentapeptide BPP5a est très instable dans le corps, une étude a démarré presque au même moment, afin de découvrir des inhibiteurs plus puissants et plus stables de cette enzyme. Un premier succès est intervenu en 1971 avec la découverte de l’action inhibitrice de l’enzyme de conversion de l’angiotensine (ECA) du nonapeptide téprotide. Le développement clinique du téprotide a cependant été arrêté deux ans plus tard par le fabricant, en raison de son intérêt commercial insuffisant.
Au début des années 1970, la structure partielle efficace des peptides inhibiteurs de l’enzyme de conversion de l’angiotensine (ECA) : le BPP5a et le téprotide a pu être établie. Ces découvertes ont permis de développer de nouveaux inhibiteurs de l’ECA non peptidiques. En 1974, l’inhibiteur de l’ECA captopril a été décrit pour la première fois : il était le produit d’un grand travail de recherche de principe actif (screening), entrepris par la société pharmaceutique Squibb. C’est en 1981 qu’il a été introduit en thérapie, comme étant le premier inhibiteur de l’ECA. Deux ans plus tard, en 1983, un deuxième inhibiteur de l’ECA, l’énalapril a été mis sur le marché.
En raison du grand succès thérapeutique et économique des médicaments à base de captopril et énalapril, une deuxième génération d’inhibiteurs de l’ECA a été développée ; elle est disponible depuis le début des années 1990; parmi ceux-ci: lisinopril et ramipril.
Importance économique
[modifier | modifier le code]En Allemagne, environ 20 % de la population et une personne de plus de 55 ans sur deux prend des médicaments pour traiter l’hypertension artérielle. Environ 35 % des patients hypertendus sont traités par un inhibiteur de l’ECA en monothérapie et environ 55 % en combinaison avec un autre médicament hypotenseur.
Aux États-Unis, 114 millions de boîtes d’inhibiteurs de l’ECA ont été prescrites en 2001. Cela correspond à un chiffre d’affaires global de 4,3 milliards de dollars US. Le lisinopril se taille la part du lion avec 47 %, suivi par l’énalapril (17 %), le captopril et le ramipril (9 % chacun). En revanche, sur le marché allemand très marqué par les génériques, c’est l’énalapril qui domine, parmi les inhibiteurs de l’ECA.
Alternatives
[modifier | modifier le code]De nouvelles substances du groupe des antagonistes des récepteurs de l'angiotensine II n’inhibent plus l’enzyme de conversion de l’angiotensine, mais agissent de manière antagoniste sur le sous-type récepteur 1 de l’angiotensine II, de sorte que les effets indésirables surviennent éventuellement plus rarement. Mais les antagonistes AT1 sont sensiblement plus onéreux que les inhibiteurs de l’ECA et n’ont pu remplacer ces derniers à ce jour. La meilleure tolérance réside dans le fait qu’ils n’interviennent pas sur le système bradykinine.
Les inhibiteurs de la vasopeptidase tels que l’omapatrilate sont dérivés des inhibiteurs de l’ECA classiques, et se trouvent actuellement en voie d’être autorisés par les autorités sanitaires. En plus d’inhiber l’enzyme de conversion de l’angiotensine, les inhibiteurs des vasopeptidases bloquent l’endopeptidase neutre, une enzyme responsable de l’inactivation du peptide natriurétique atrial (ANP) vasodilatateur.
Un autre point innovant d’intervention est l’inhibition de la rénine, une enzyme formée dans le rein, qui est responsable de la synthèse de l’angiotensine I. Un premier inhibiteur sélectif de la rénine, l'aliskirène, est commercialisé depuis 2007, puis retiré du marché en 2017[15].
En médecine vétérinaire, le pimobendane (pimobendan) a démontré une efficacité supérieure aux IECA pour le traitement de l'insuffisance cardiaque canine congestive.
Aspect médecine intensive
[modifier | modifier le code]En soins intensifs, il a été montré que les patients ayant été traités par les inhibiteurs de l’ECA avant leur séjour en unité de soins intensifs, présentent souvent une consommation accrue de catécholamines, pour stabiliser la pression artérielle moyenne. La raison devrait être un déficit en vasopressine, qui serait à attribuer à la thérapie précédente par les inhibiteurs de l’ECA. La substitution de la vasopressine, plus particulièrement chez les patients se trouvant dans une situation délicate concernant la catécholamine, permet souvent de réduire rapidement le besoin en catécholamine (dans la mesure où il n’existe aucun autre motif d’avoir une pression artérielle plus basse et d’équilibrer ensuite la vasopressine en l’espace de 12-24 heures).
En savoir plus
[modifier | modifier le code]Notes et références
[modifier | modifier le code]- ↑ James M. Wright, Vijaya M. Musini et Rupam Gill, « First-line drugs for hypertension », The Cochrane Database of Systematic Reviews, vol. 4, no 4, , p. CD001841 (ISSN 1469-493X, PMID 29667175, PMCID 6513559, DOI 10.1002/14651858.CD001841.pub3, lire en ligne, consulté le )
- ↑ WeiPing Sun, HaiBin Zhang, JinCheng Guo et XueKun Zhang, « Comparison of the Efficacy and Safety of Different ACE Inhibitors in Patients With Chronic Heart Failure: A PRISMA-Compliant Network Meta-Analysis », Medicine, vol. 95, no 6, , e2554 (ISSN 1536-5964, PMID 26871774, PMCID 4753869, DOI 10.1097/MD.0000000000002554, lire en ligne, consulté le )
- ↑ Sorbets E, Labreuche J, Simon T et al. Renin-angiotensin system antagonists and clinical outcomes in stable coronary artery disease without heart failure, Eur Heart J, 2014;35:1760-1768
- ↑ Yusuf S, Sleight P, Pogue J, Bosch J, Davies R, Dagenais G, Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patientsThe Heart Outcomes Prevention Evaluation Study Investigators, N Engl J Med, 2000;342:145–153
- ↑ Fox KM, EURopean trial On reduction of cardiac events with Perindopril in stable coronary Artery disease Investigators, Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicentre trial (the EUROPA study), Lancet, 2003;362:782–788
- ↑ Teo KK, Burton JR, Buller CE et al. Long-term effects of cholesterol lowering and angiotensin-converting enzyme inhibition on coronary atherosclerosis: the Simvastatin/Enalapril Coronary Atherosclerosis Trial (SCAT), Circulation, 2000;102:1748–1754
- ↑ Savarese G, Costanzo P, Franklin Cleland JG et al. A meta-analysis reporting effects of angiotensin-converting enzyme inhibitors and angiotensin receptor blockers in patients without heart failure, J Am Coll Cardiol, 2013;61:131-142.
- Mingkwan Na Takuathung, Wannachai Sakuludomkan, Rapheephorn Khatsri et Nahathai Dukaew, « Adverse Effects of Angiotensin-Converting Enzyme Inhibitors in Humans: A Systematic Review and Meta-Analysis of 378 Randomized Controlled Trials », International Journal of Environmental Research and Public Health, vol. 19, no 14, , p. 8373 (ISSN 1660-4601, PMID 35886227, PMCID 9324875, DOI 10.3390/ijerph19148373, lire en ligne, consulté le )
- ↑ Thériaque est une banque de données sur tous les médicaments disponibles en France, destinée aux professionnels de santé., « Effets indésirables à dose thérapeutique : TROUBLES RESPIRATOIRES », sur theriaque.org (consulté le ).
- ↑ Cooper WO, Hernandez-Diaz S, Abrogast PG et al. Major congenital malformations after first-trimester exposure to ACE inhibitors, N Engl J Med, 2006;354:2443-51
- ↑ Li D-K, Yang C, Andrade S, Tavares V, Ferber JR, Maternal exposure to angiotensin converting enzyme inhibitors in the first trimester and risk of malformations: a retrospective cohort study, BMJ, 2011;343:d5931
- ↑ Nida Buawangpong, Supanimit Teekachunhatean et Nut Koonrungsesomboon, « Adverse pregnancy outcomes associated with first-trimester exposure to angiotensin-converting enzyme inhibitors or angiotensin II receptor blockers: A systematic review and meta-analysis », Pharmacology Research & Perspectives, vol. 8, no 5, , e00644 (ISSN 2052-1707, PMID 32815286, PMCID 7438312, DOI 10.1002/prp2.644, lire en ligne, consulté le )
- ↑ Hicks BM, Filion KB, Yin H, Sakr L, Udell JA, Azoulay L, Angiotensin converting enzyme inhibitors and risk of lung cancer: population based cohort study, BMJ, 2018;363:k4209
- ↑ Lapi F, Azoulay L, Yin H, Nessim SJ, Suissa S, Concurrent use of diuretics, angiotensin converting enzyme inhibitors, and angiotensin receptor blockers with non-steroidal anti-inflammatory drugs and risk of acute kidney injury: nested case-control study, BMJ, 2013;346:e8525
- ↑ « Spécialités d'aliskiren : déremboursement de RASILEZ et RASILEZ HCT à l'automne »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur VIDAL (consulté le ).
